Vedi traduzione automatica
Questa è una traduzione automatica. Per vedere il testo originale in inglese cliccare qui
#Tendenze
Il passato e il presente dei PARPis
Il passato e il presente dei PARPis
Nel 2014 è stato lanciato il primo inibitore di PARP (Olaparib). Si tratta del primo farmaco commercializzato secondo il concetto di letalità sintetica, che ha aperto una nuova strada per la terapia mirata ai tumori.
Gli inibitori di PARP e il loro meccanismo
Il nome completo degli inibitori PARP è inibitori della poliadenosina difosfato ribosio polimerasi.
Nel 1922, Calvin Bridges, un genetista che lavorava nel Morgan Laboratory della Columbia University, scoprì che la morte della drosofila si verificava quando due geni specifici della drosofila venivano inattivati contemporaneamente, mentre l'inattivazione mutazionale di uno solo di questi due geni non provocava danni fatali alla drosofila. La cosiddetta "letalità sintetica" significa che per due geni in una cellula, quando uno di essi è mutato da solo o non funziona, non causerà la morte della cellula; e quando entrambi sono mutati o non possono essere espressi, porterà alla morte della cellula. Questo principio permette di uccidere selettivamente le cellule tumorali senza intaccare le cellule somatiche normali.
Nel 2005, due studi pubblicati contemporaneamente da Nature hanno confermato per la prima volta l'esistenza di un effetto letale sintetico tra gli inibitori PARP e le mutazioni BRCA1/2.
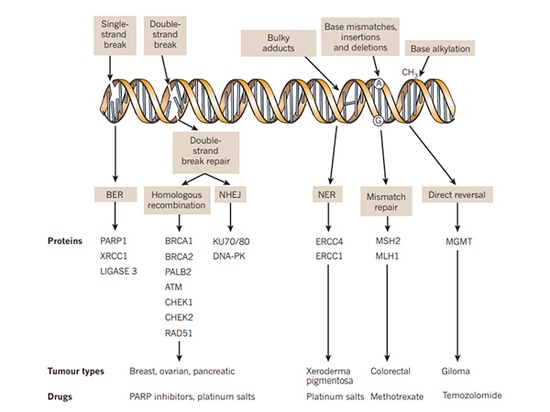
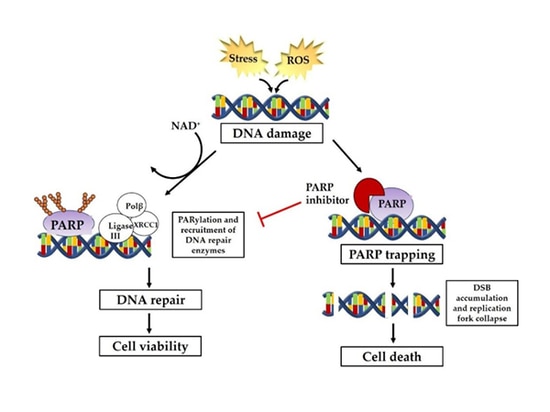
Le vie coinvolte nella riparazione del DNA comprendono principalmente la riparazione delle rotture a singolo filamento (SSBR) e la riparazione delle rotture a doppio filamento (DSBR). I meccanismi di riparazione includono principalmente la ricombinazione omologa (HR), la giunzione delle estremità non omologhe (NHEJ), la riparazione per escissione di basi (BER), la riparazione per escissione di nucleotidi (NER), la riparazione di mismatch (MMR) e la sintesi di transioni, ecc. Tra questi, la riparazione del DNA a singolo filamento dipende dalla via di riparazione mediata da PARP. Quando il DNA a singolo filamento è danneggiato, PARP si riunisce nel sito di rottura del DNA a singolo filamento e viene attivato, reclutando quindi una serie di complessi per partecipare alla riparazione del DNA. Gli inibitori di PARP inibiscono l'attività dell'enzima PARP per impedirgli di funzionare formando polimeri PAR per attirare le proteine correlate alla riparazione del danno al DNA. La riparazione per ricombinazione omologa (HRR) è il metodo di riparazione preferito per le rotture del doppio filamento di DNA. I pazienti con deficit di riparazione della ricombinazione omologa (HRD), causato da mutazioni del gene HRR, tra cui mutazioni BRCA nelle cellule tumorali, mutazioni germinali, mutazioni somatiche di geni correlati riparati dalla ricombinazione omologa, inattivazione epigenetica e molti altri fattori, perdono la funzione di riparazione delle rotture del doppio filamento del DNA, con conseguente incapacità di riparare sia il singolo filamento che il doppio filamento delle cellule tumorali per ottenere la letalità sintetica.
Inibitori di PARP approvati
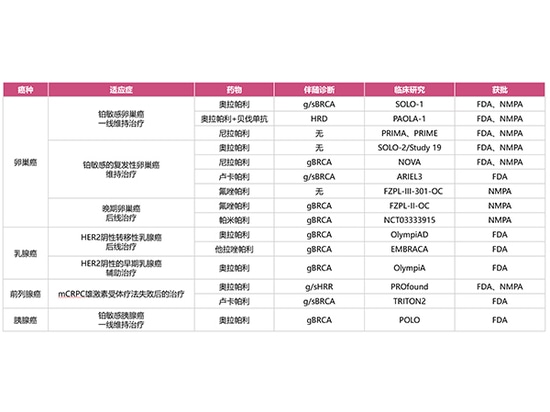
Attualmente, la FDA statunitense ha approvato 4 inibitori di PARP (Olaparib, Niraparib, Rucaparib e Talazoparib), mentre l'NMPA cinese ha approvato 4 inibitori di PARP (Olaparib, Niraparib, Fluzoparib, Pamiparib), che sono stati applicati clinicamente al cancro ovarico, al seno, al pancreas e alla prostata.
Indicazioni applicabili approvate dalla FDA:
Orapali:
È utilizzato per il trattamento di mantenimento di pazienti con carcinoma ovarico avanzato g/s BRCA-mutato che hanno raggiunto la CR/PR dopo la chemioterapia di prima linea a base di platino;
Per il trattamento di mantenimento di pazienti con carcinoma ovarico ricorrente sensibile al platino che hanno raggiunto la CR/PR dopo la chemioterapia di prima linea a base di platino;
Per il trattamento di mantenimento combinato con bevacizumab di pazienti con carcinoma ovarico avanzato HRD-positivo che hanno raggiunto CR/PR dopo chemioterapia di prima linea a base di platino;
Per la terapia adiuvante di pazienti adulte con carcinoma mammario precoce ad alto rischio mutato in gBRCA HER2-negativo che hanno ricevuto una chemioterapia neoadiuvante o adiuvante;
Per il trattamento di pazienti adulte con carcinoma mammario metastatico mutato in gBRCA, HER2-negativo, sottoposte a chemioterapia neoadiuvante o adiuvante;
Per il trattamento di mantenimento di pazienti con adenocarcinoma pancreatico metastatico che non hanno progredito con un regime di chemioterapia di prima linea a base di platino per almeno 16 settimane e che presentano mutazioni di gBRCA;
Per il trattamento di pazienti adulti con carcinoma prostatico metastatico resistente alla castrazione (mCRPC) mutato nel gene g/s HRR che hanno avuto una progressione dopo aver ricevuto enzalutamide o abiraterone prima della terapia staminale.
Nirapali
È utilizzato per il trattamento di mantenimento di prima linea di pazienti con carcinoma ovarico avanzato che hanno raggiunto la CR/PR con la chemioterapia di prima linea a base di platino;
Per il trattamento di mantenimento di pazienti con carcinoma ovarico ricorrente sensibile al platino
Lucapali
È utilizzato per il trattamento di mantenimento di pazienti con carcinoma ovarico ricorrente sensibile al platino;
Per il trattamento di pazienti adulti con carcinoma prostatico metastatico resistente alla castrazione (mCRPC) che hanno ricevuto in precedenza una terapia mirata al recettore degli androgeni e una chemioterapia con taxani e che presentano mutazioni del gene BRCA.
Talazoparib
È utilizzato per il trattamento di pazienti con mutazione gBRCA, HER2-negativi, con carcinoma mammario localmente avanzato o metastatico.
Indicazioni applicabili approvate dall'ANMP:
Orapali
È utilizzato per il trattamento di mantenimento di pazienti con carcinoma ovarico ricorrente sensibile al platino;
Per il trattamento di mantenimento di prima linea di pazienti con carcinoma ovarico avanzato con mutazione BRCA;
Per la terapia di mantenimento di prima linea combinata con bevacizumab per le pazienti con carcinoma ovarico avanzato di nuova diagnosi che hanno ricevuto una remissione completa o parziale dopo chemioterapia a base di platino e sono positive all'HRD;
Per la monoterapia di pazienti adulti con carcinoma prostatico metastatico resistente alla castrazione portatori di mutazioni BRCA1/2 (germline e/o somatiche) e progressione della malattia dopo un precedente trattamento con nuovi farmaci ormonali.
Nirapali
È utilizzato per il trattamento di mantenimento di pazienti con carcinoma ovarico ricorrente sensibile al platino dopo che la chemioterapia contenente platino ha ottenuto una remissione completa o parziale;
Per la terapia di mantenimento di prima linea di pazienti con carcinoma ovarico avanzato che hanno ottenuto una risposta completa o parziale alla chemioterapia di prima linea a base di platino.
Fluzoparib
È utilizzato per il trattamento di pazienti con carcinoma ovarico ricorrente sensibile al platino con mutazione gBRCA che hanno ricevuto una chemioterapia di seconda linea o più;
Per il trattamento di mantenimento di pazienti con carcinoma ovarico ricorrente sensibile al platino dopo la remissione completa o parziale della chemioterapia a base di platino.
Pamipali
È utilizzato per il trattamento di pazienti con carcinoma ovarico avanzato, carcinoma delle tube di Falloppio o carcinoma peritoneale primario che hanno ricevuto almeno due linee di chemioterapia e mutazione gBRCA.
Indicazioni applicabili ritirate dall'FDA:
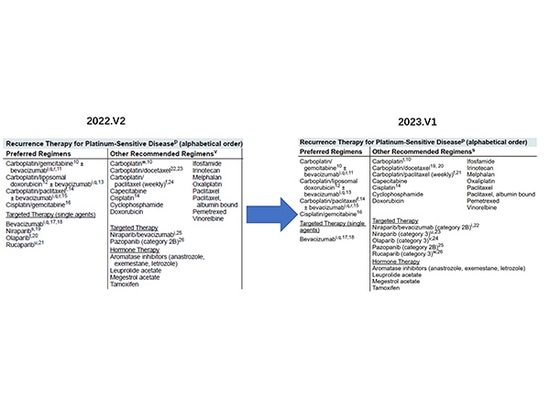
Con il continuo aggiornamento della ricerca clinica, i dati clinici dimostrano che il rischio di morte delle pazienti affette da carcinoma ovarico che utilizzano lucaparib, olaparib e niraparib è aumentato, per cui l'FDA ha ritirato alcune delle indicazioni pertinenti, tra cui il restringimento delle indicazioni per la terapia di mantenimento di seconda linea da parte di niraparib è il più evidente, e anche le linee guida NCCN sono state adattate nel tempo per rimuovere la raccomandazione corrispondente e abbassare il livello di raccomandazione.
1. Nel giugno 2022, l'FDA ha ritirato rucaparib per il trattamento di seconda linea delle pazienti con carcinoma ovarico BRCA-mutato.
2. Nell'agosto 2022, l'FDA ha ritirato olaparib per il trattamento tardivo di pazienti con carcinoma ovarico avanzato con mutazioni BRCA.
3. Nel settembre 2022, l'FDA ha ritirato niraparib per il trattamento in seconda linea di pazienti adulti con mutazioni BRCA, carcinoma ovarico epiteliale ricorrente HRD-positivo e sensibile al platino, carcinoma delle tube di Falloppio o carcinoma peritoneale primario.
4. Nel novembre 2022, l'FDA ha ritirato alcune indicazioni per il trattamento di mantenimento con niraparib per le pazienti con carcinoma ovarico ricorrente sensibile al platino.
Nel marzo 2021, i dati di OS (sopravvivenza globale) di uno studio NOVA che utilizzava niraparib come terapia di mantenimento in pazienti con carcinoma ovarico ricorrente sensibile al platino hanno mostrato che per le pazienti con mutazioni non BRCA, l'OS mediana nel gruppo niraparib è stata di 31,1 mesi, rispetto ai 36,5 mesi del gruppo di controllo, il che significa che non vi è alcun beneficio in termini di OS dalla terapia di mantenimento con niraparib. Nel risultato finale di OS dello studio NOVA, l'hazard ratio (HR) di OS per i pazienti senza mutazioni BRCA è stato di 1,10 (95% CI: 0,831-1,459).
Nel settembre 2022, l'American Society of Clinical Oncology (ASCO) ha lanciato "PARP Inhibitor Ovarian Cancer Management: ASCO Guideline Rapid Recommendation Update", in cui si sottolinea che per le pazienti con carcinoma ovarico ricorrente non mutato in BRCA, la terapia di mantenimento con niraparib deve essere soppesata tra il potenziale beneficio in termini di PFS (sopravvivenza libera da progressione) e la riduzione della OS.
Ora, con il ritiro delle indicazioni parziali degli inibitori di PARP, l'uso clinico degli inibitori di PARP è relativamente calmo e c'è anche la richiesta di una guida precisa per i farmaci.
Sintesi
Gli inibitori di PARP sono farmaci mirati che esercitano effetti antitumorali attraverso l'effetto "letale sintetico" sulla base della HRD. Il suo avvento ha cambiato il modello di trattamento del carcinoma ovarico, rendendo la terapia di mantenimento una parte importante della gestione complessiva del carcinoma ovarico, che ha un significato miliare.
Nella pratica clinica, le indicazioni per l'uso degli inibitori di PARP devono essere rigorosamente colte. Si raccomanda di rilevare di routine le mutazioni del gene BRCA prima della terapia, e di eseguire la rilevazione dell'HRD se le condizioni lo consentono, in modo da guidare accuratamente la terapia clinica e valutare la prognosi.
Tra le indicazioni degli inibitori PARP, oltre al tumore della mammella, dell'ovaio, delle tube di Falloppio, ecc. anche il tumore della prostata, che è anche un tumore riproduttivo, ha un grande entusiasmo per la ricerca e lo sviluppo, e la terapia di combinazione è anche un importante hotspot di ricerca. In futuro, con la conclusione di un maggior numero di studi clinici, gli scenari di applicazione clinica degli inibitori di PARP e dei relativi marcatori molecolari diventeranno sempre più chiari.
riferimenti:
1. Linee guida per l'applicazione clinica degli inibitori di PARP nel carcinoma ovarico (edizione 2022)
2. Nature. 2012 Jan 18;481(7381):287-94.
3. J Clin Med. 2019 Mar 30;8(4):435.
4. Sito ufficiale della FDA
5. Sito ufficiale dell'NMPA
6. Linee guida NCCN